足交 3000+高清大脑细胞基因组图谱!北大谢晓亮团队访谈实录 | CellPress对话科学家
 足交
足交
来源: CellPress细胞科学
2021年1月23日,来自北京大学生物学前沿窜改中心主任,谢晓亮陶冶团队在细胞出书社旗下期刊Cell上在线发表了题为Changes in genome architecture and transcriptional dynamics progress independently of sensory experience during post-natal brain development 的探求,带来了进步3000个哺乳动物脑细胞的转录组图集和三维基因组图集。这些数据可以为神经发育以及相关疾病的诊疗提供匡助。
Cell Press细胞出书社微信公众号对该论文作家团队进行了采访并对论文进行了解读,旨在与强盛科研东说念主员潜入共享该探求恶果以及一些将来的瞻望。
探求摘录
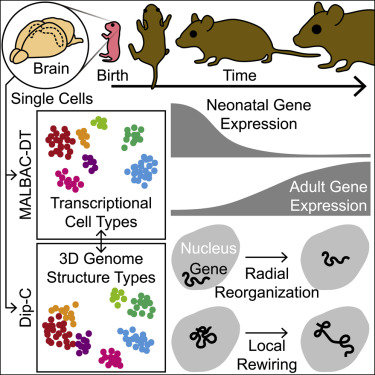
哺乳动物基因组的转录和三维(3D)结构在神经发育和发育艰辛中阐扬着至关贫穷的作用。然则,单个脑细胞的3D基因组结构如故未知,探求界对出死后的单细胞转录组和3D基因组动态也了解很少。在此,咱们利用了高分辨率的“用于数字转录组分析的屡次退火环状轮回扩增本领”(MALBAC-DT)和“二倍体染色质构象拿获”(Dip-C)轨范,生成了正在发育的小鼠皮层和海马体的转录组(3,517个细胞)和3D基因组(3,646个细胞)图谱。在成年小鼠中,3D基因组“结构类型”刻画了总共主要细胞类型,染色质A/B区室化与基因抒发之间存在很高的相关性。在发育历程中,转录组和3D基因组在出死后第一个月均发生庸碌的回荡。在神经元中,3D基因组大范围再行组合,这一欢跃与基因抒发模块相关,但与感官体验无关。临了,咱们探究了萍踪基因的等位基因特异性结构,揭示了局部和染色体(chr)范围的互异。这些发现揭示了神经发育的未知维度。
Cell Press细胞出书社特别邀请谢晓亮陶冶及谭隆志博士进行了专访,请他为大师进一步稳当解读。
CellPress:
请您先容一下探求布景和初志。
谢晓亮陶冶:
咱们团队一直竭力于单个细胞基因调控与3D基因组结构的探求。在东说念主体的每一个细胞里,总长达2米的46条染色体具有相当稀奇的3D结构,能通过改变不同基因的体式来调控它们的抒发。
此前,为了探求单细胞的3D基因组结构,咱们团队的谭隆志博士等东说念主于2018年迷惑了一项名为Dip-C的单细胞测序本领,初次取得单个东说念主类细胞的高分辨率全基因组3D结构。直到今天,Dip-C如故高分辨率测量单细胞3D全基因组结构的唯独轨范,其分辨率比当今来源进的显微成像轨范还要高两个数量级,现实操作也相当简便、资本极低。
尔后的2019年,咱们操纵Dip-C探求了小鼠嗅觉神经元——鼻腔里的嗅嗅觉神经元、视网膜上的视杆细胞——极其特殊的3D基因组结构尽头发育历程。本探求则更进一步、径直探索小鼠的神经核心:大脑。
谭隆志博士:
基因组的结构与转录对东说念主类健康相当贫穷,在大脑的发育中尤其如斯。许多神经发育相关疾病——比如自闭症与精神分裂症——都与基因组3D结构与转录失调相关。然则,畴昔的本领无法测量单个细胞的3D基因组结构。即便在单细胞转录组层面,此前也莫得哺乳动物大脑产后发育的数据。这些本领难关严重阻挠了神经发育及相关疾病的探求。本探求初次测量了哺乳动物大脑在产后发育中单细胞3D基因组结构与转录组,为神经发育探求提供了可贵资源、为神经疾病的会诊与调养提供了新念念路。
CellPress:
能否简要先容本探求接收的MALBAC-DT轨范尽头主要上风?
谢晓亮陶冶:
MALBAC-DT是咱们团队于2020年头新研发的单细胞转录组测序轨范,领有极高的贤达度和准确度。它的旨趣是基于咱们团队早在2012年就已发表的高着力全基因组扩增轨范MALBAC。咱们曾在2015年将MALBAC应用于RNA,取得了可以的完了。四肢这一系列的最新恶果,MALBAC-DT在各个方面比拟MALBAC RNA都有了巨大的擢升,对RNA分子的扩增更高效、对抒发量的测量也更准确。尤其值得一提的是足交,咱们通过严谨的现实筹划,幸免了市面上绝大部分单细胞转录组测序轨范都存在的RNA分子数量误测,让完了更接近信得过。
谭隆志博士:
本探求中,咱们初次将MALBAC-DT应用于单个细胞核,从而幸免索取竣工细胞时对细胞气象的不良影响。测序完了标明,MALBAC-DT确实能高效测量基因抒发,检测到的RNA分子数量比以往探求小鼠大脑皮层发育的著作要多一个数量级。是以此次的转录组图谱质料相当高,更能揭示大脑发育中基因的动态抒发。
CellPress:
成年小鼠和更生小鼠的神经元类型及3D基因组气象有哪些互异?
谢晓亮陶冶:
咱们的MALBAD-DT和Dip-C数据标明,成年小鼠与更生小鼠大脑细胞在分子层面存在巨大互异。固然更生小鼠已具有险些总共的神经元类型,但其转录组却和对应的成年神经元不一样。一些基因只在更生神经元中抒发,而另一些基因却在成年神经元中抒发更高。咱们把这些基因统称为更生与成年共抒发模组。
谭隆志博士:
在3D基因组层面,成年小鼠的大脑神经元与更生神经元互异相当较着,看起来就像两种十足不同的细胞类型。大程序上,咱们发现基因组许多区域平时处在细胞核名义,却在神经元分化历程中大幅向细胞核里面出动;比如小鼠的7号染色体(主要对应东说念主类19号等染色体)就险些整条染色体内移。小程序上,许多基因的染色质A/B区室都发生了变化,它们的增强子-启动子DNA环也跟着发育改变体式。
CellPress:
本探求若何通过嗅觉抢劫实考解释了3D基因组回荡是基因上事前敬佩的?
谢晓亮陶冶:
本探求中,咱们用Dip-C轨范发现大脑3D基因组结构在产后发生巨大变化。这一行化恰好发生在大脑启动给与外界感官刺激的时代,即小鼠出死后的第一个月。因此,一个相当贫穷的问题是:这些分子层面的变化是由外界感官刺激引起的吗?
谭隆志博士:
咱们以视觉为例来探求这个问题。小鼠出死后,约12天睁开眼睛看宇宙。咱们将出身的小鼠在迷蒙中饲养,这么它们就不会受到任何视觉刺激。有兴味的是,这些小鼠视觉皮层的3D基因组险些不受影响、依然时时回荡。这讲明3D基因组的变化是先天决定的、不受后天影响。
CellPress:
不同功能的神经元在不同的大脑部位和/或发育阶段阐扬出不同的功能属性,为什么?
谢晓亮陶冶:
不同的大脑部位有相当不同的意志功能,其中的神经元也阐扬出多样稀奇的口头、电生理、邻接特色。这些功能属性的变成都取决于神经元稀奇的基因抒发。本探求初次得到哺乳动物大脑产后发育的单细胞转录组与3D基因组图谱,为探求神经元变成不同功能属性的分子基础提供了贫穷数据。
谭隆志博士:
更生儿与成年东说念主的念念维、悲痛相当不一样。不同发育阶段的大脑,介意志功能和可塑性方面也有很大的区别。咱们的数据标明,哪怕是在产后,不同发育阶段的神经元在基因组结构与抒发上也有巨大辞别。这些分子层面的变化很可能决定了大脑功能的变化,为更生与成年大脑的功能区别提供全新的解释。
CellPress:
3D基因组“结构类型”与相应的转录组类型存在何如的关系?
谢晓亮陶冶:
早在2018年,咱们团队就发现:仅通过单细胞3D基因组结构,就能辩认东说念主血中的主要细胞类型。因此,就像大师常说的细胞转录组类型,咱们把不同的单细胞基因组结构称为“结构类型”。2019年咱们探求小鼠的鼻子与眼睛,印证了这一论断。但是比起这些组织,大脑的细胞转录组类型要复杂得多,因此也更有挑战性。
谭隆志博士:
为了惩处大脑细胞转录组与基因组结构的关系这一难题,咱们迷惑了全新的数据分析轨范、系统地将单细胞转录组类型与3D结构类型逐个双应。咱们发现,在转录组类型中特异抒发的基因,其单细胞染色质A/B区室(咱们称为scA/B)也会在对应的结构类型里特他乡偏向A区室(即愈加洞开、愈加真染色质)。这一稀奇算法让咱们见效辩认大脑里多样不同神经元的3D结构类型。
CellPress:
大脑神经元和OSN在基因构成和3D基因组回荡方面有哪些相似之处和贫穷互异?该若何解释这些互异?
谢晓亮陶冶:
咱们团队从2013年起,就一直探求OSN稀奇的单细胞基因抒发与3D结构、并发表一系列著作。咱们发现每个OSN之是以能只抒发单一OR基因,是归功于它们特殊的3D基因组结构:包括OR基因在内许多区域平时处在细胞核名义,却在OSN分化历程中大幅向细胞核里面出动、多条染色体之间邃密无比连结在一王人,共同千里默这些OR基因。与此同期,不同染色体上的OR基因增强子也连结起来,变成数个增强子环节,共同调控单一抒发的OR。
谭隆志博士:
弥远以来,OSN的这一3D结构一直被合计仅仅一个特例、莫得普适性。本探求中,咱们却只怕发现,OSN中内移的基因组区域(包括OR基因),在成年大脑神经元里也险些雷同地移向细胞核的中心。但与OSN不同的是,不但OR和OR之间有染色体互相作用,其他访佛的区域(包括免疫球卵白在内的其他基因眷属)也产生了互相作用;与此相背,OR增强子在大脑中却不再互相作用。在OSN中调控3D结构的基因(如转录因子与核纤层相关卵白),在大脑神经元里也有不尽交流的抒发特色。这讲明核心与周围神经系统的发育既有共通之处,也有略有不同的分子机制。这一论断标明,OSN因为易于取样、终身可再生,将为神经发育疾病的会诊与调养提供可贵材料。
CellPress:
本探求还惩处了基因组学领域的哪些难题?
谢晓亮陶冶:
固然在咱们和其他团队的用功下,当今已出现不少单细胞3D基因组轨范和数据,但相关的数据分析算法还很有限,与其他单细胞组学数据的整合轨范也险些为零。
谭隆志博士:
咱们新迷惑的Dip-C数据分析轨范,恰恰惩处了这一逆境。如上所述,咱们的算法能整合分析单细胞与老例3D基因组、转录组、DNA甲基化组、洞开染色质等数据,可以庸碌应用于其他生物系统的探求足交,如癌症、器官发生、学习与悲痛、病弱与神经退行等。
